Levitra enthält Vardenafil, das eine kürzere Wirkdauer als Tadalafil hat, dafür aber schnell einsetzt. Männer, die diskret bestellen möchten, suchen häufig nach levitra kaufen ohne rezept. Dabei spielt die rechtliche Lage in der Schweiz eine wichtige Rolle.
Formazioneveterinaria.it
AGGIORNAMENTI IN MEDICINA VETERINARIA :questioni di clinica medica degli
animali da compagnia
Diagnosi caso 1: Il cane magro con il "pancione": un segno, tante cause
Grazie alla raccolta anamnestica, la visita clinica e le indagini collaterali è stato possibile raggiungere la diagnosi di sospetto: epatite cronica di origine tossica causata dall'ingestione di parti velenose di
Cycas Revoluta. Le epatiti croniche del cane, sono processi flogistici che si sviluppano principalmente a livello del parenchima epatico, con il conseguente innalzamento dei valori delle transaminasi. Si tratta di patologie che si riscontrano soprattutto in cani di età adulta (4-7 anni) ad eccezione delle forme ereditarie da accumulo di rame che possono insorgere anche in soggetti più giovani; risultano maggiormente interessate le femmine, e, pur potendo interessare tutte le razze, esiste maggiore predisposizione per Bedlington Terrier, Dalmata, Labrador Retriever, Whest Highland White Terrier, Dobermann e Spaniel. Dal punto di vista sintomatologico, i cani affetti da epatite cronica possono presentarsi asintomatici o con segni clinici del tutto aspecifici, quali poliuria e polidipsia, anoressia/disoressia, dimagramento, abbattimento e intolleranza agli sforzi, vomito, diarrea e nei, casi gravi, ascite, coagulopatie ed encefalopatia epatica. La visita clinica del paziente raramente porta al riscontro di qualche reperto indicativo ad eccezione di uno scadimento delle condizioni generali del soggetto, o condizioni più eclatanti come ittero o ascite. Anche le alterazioni di laboratorio risultano non sempre indicative: si riscontrano di norma aumenti delle transaminasi , meno costanti aumenti di fosfatasi alcalina e γ-glutamiltransferasi; nelle fasi avanzate è poi possibile evidenziare tutte le alterazioni indicative di un malfunzionamento epatico, come ipoalbuminemia, riduzione dei valori dell'urea, aumento degli acidi biliari, abbassamento del fibrinogeno. Tra le alterazioni ematologiche che si possono incontrare, ci sono lieve anemia, leucocitosi e piastrinopenia (da consumo, in associazione a coagulopatia) oltre all'aumento dei tempi coagulativi (tempo di protrombina (PT), e tempo di tromboplastina parziale, PTT). La diagnostica per immagini, ed in particolare l'ecografia addominale, può solo completare il quadro ma non fornisce la diagnosi di certezza, in quanto possono sia essere evidenziate alterazioni nella struttura epatica, soprattutto in caso di cirrosi, ma non necessariamente soggetti affetti da epatite cronica presentano alterazioni dell'ecostruttura rilevabili all'esame. Lo strumento diagnostico più indicato in caso di tali patologie, è rappresentato dall'esame istopatologico di un campione prelevato tramite biopsia (ovviamente va ricordato che, in caso di patologia avanzata, in cui fossero comparsi deficit coagulativi, quest'ultima risulta controindicata). Nel presente caso l'esame bioptico ed istopatologico non è stato eseguito in quanto il proprietario non ha dato il suo consenso alla procedura perché preoccupato degli elevati rischi anestesiologici dovuti alla grave condizione clinica del suo cane.
Le cause alla base dell'epatite cronica nel cane sono spesso sconosciute, è per questo motivo che molte di queste patologie sono classificate come idiopatiche, sebbene si sia ipotizzata un'origine autoimmune; tra le cause note di epatite si possono considerare quelle tossiche, quelle infettive (batteriche, virali o protozoarie), le ereditarie (da accumulo di rame). L'approccio terapeutico in corso di epatite cronica è duplice: terapie specifiche, volte ad eliminare la causa primaria e aspecifiche, per contrastare gli effetti negativi che si verificano a livello epatico in corso della patologia. Qualora non sia possibile risalire alla causa sottostante la terapia è solo sintomatica per eliminare l'infiammazione, rallentare i processi di fibrosi, antagonizzare gli effetti ossidativi ed evitare la colestasi. Nel caso clinico descritto non è stato possibile raggiungere una diagnosi di certezza e, nonostante il forte sospetto di una origine tossica dell'epatite cronica in atto, la terapia instaurata è stata solo sintomatica sia perché non è documentata l'esistenza di un antidoto efficace nei confronti delle tossine della Cycas sia per l'eccessivo lasso di tempo intercorso dall'ingestione di tali sostanze. Il cane è stato quindi trattato con: - Fluidoterapia - Diuretici (furosemide alla dose di 2-4 mg/kg , bid, per via orale) - Antibiotico terapia (amoxicillina/acido clavulanico alla dose di 20 mg/kg, bid, per os) -Alimento complementare specifico con Silimarina, MOS e fosfatidilcolina -Integrazione di vitamine del gruppo B -Dieta specifica per patologie epatiche Il soggetto ha mostrato un lieve miglioramento clinico all'inizio del trattamento dovuto alla riduzione dell'ascite. Purtroppo dopo circa 3 settimane si è verificato un progressivo peggioramento della sintomatologia fino al decesso.
Diagnosi caso 2 : Il boxer con il "gonfiore" alle zampe: non sempre è un problema di
Considerando la presenza di alcuni segni clinici suggestivi (linfoadenomegalia, splenomegalia, anemia, proteinuria….) e che Bella è nata ed è vissuta sempre in area endemica per leishmaniosi , i successivi esami diagnostici sono stati indirizzati per la valutazione di tale patologia. La diagnosi eziologica di leishmaniosi canina è possibile mettendo in evidenza il protozoo o gli anticorpi diretti contro di esso. I metodi diagnostici utilizzabili sono: l'osservazione diretta al microscopio di un preparato citologico ottenuto da ago-aspirato linfonodale, midollare, splenico o da campioni citologici ottenuti da lesioni campionabili (es.: lesioni nodulari, scarificazioni di lesioni ulcerate cutanee, ecc…) che permette l'identificazione degli amastigoti di Leishmania infantum; test sierologici (test rapidi immunocromatografici, ELISA, immunofluorescenza) eseguiti su siero di sangue per la messa in evidenza di anticorpi- anti Leishmania infantum; test PCR (qualitativo o quantitativo) eseguito su sangue midollare, materiale linfonodale, materiale splenico, materiale ottenuto da lesioni cutanee attribuibili al parassita o sangue periferico, per l'amplificazione del DNA del protozoo; esame colturale (facilmente ottenibile da materiale linfonodale) che permette la moltiplicazione del parassita e la valutazione della presenza dello stesso sottoforma di promastigote. Tale tecnica richiede lunghi tempi di attesa, circa 4 settimane, e per tale motivo non è utilizzabile a scopo diagnostico ambulatoriale.
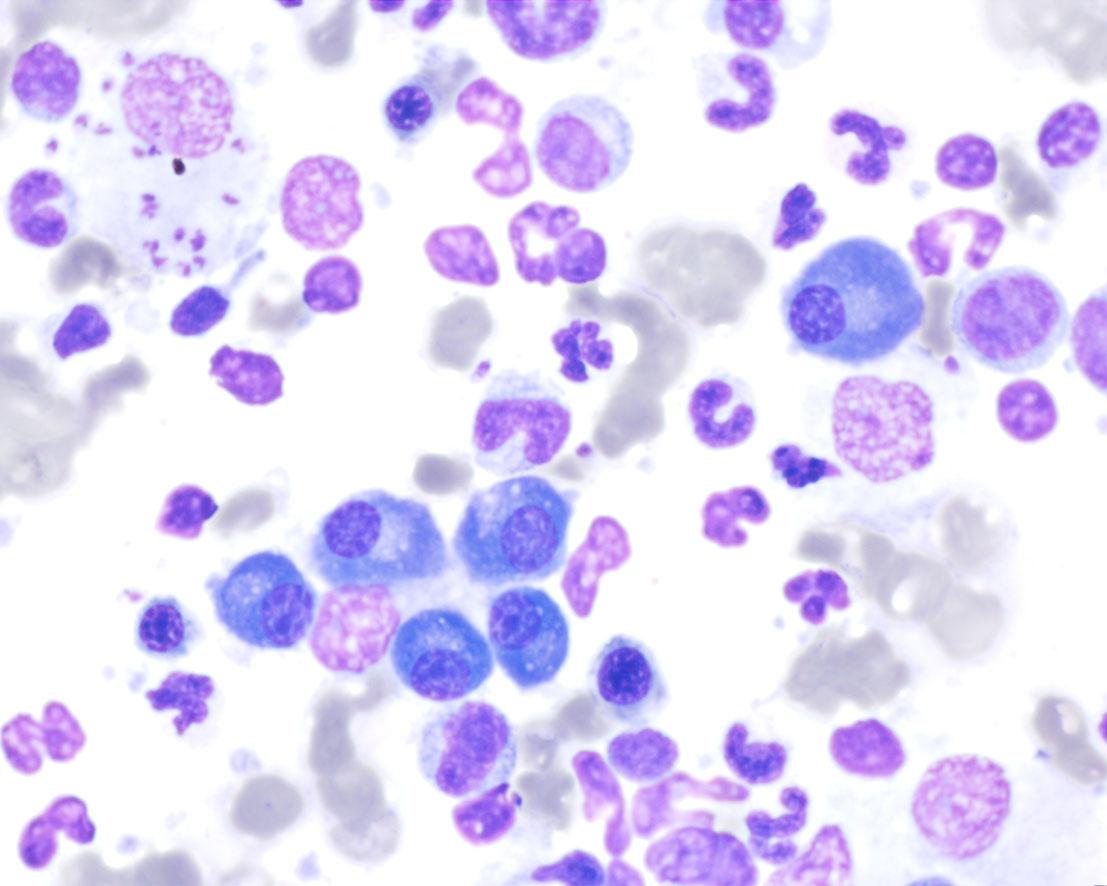
Nel caso di Bella è stato deciso di eseguire un prelievo di sangue per l'esecuzione del test IFAT e, in attesa dei risultati, un ago-aspirato midollare a livello delle sternebre per una più rapida ricerca del parassita. L'osservazione diretta al microscopio dei preparati citologici midollari ha permesso l'identificazione di numerosi amastigoti di L. infantum, sia all'interno dei macrofagi sia in sede extracellulare (Fig.3).
Figura 1 Preparato citologico midollare. Numerosi amastigoti di L. infantum all'interno di un macrofago (Freccia grande). Sono evidenti numerose plasmacellule (Freccia piccola). Questo reperto ha permesso di emettere una diagnosi certa di leishmaniosi. Il successivo esito del test IFAT ha messo in evidenza la presenza di un elevato titolo anticorpale pari a 1/2560. Prima di iniziare il trattamento terapeutico di un cane affetto da leishmaniosi è importantissimo cercare di inquadrare l'infezione-malattia nel suo stadio evolutivo, sia per consentirne l'opportuna terapia, sia per anticipare possibili evoluzioni verso fasi più gravi o di irreversibilità. Le più recenti linee guida pubblicate dal gruppo di studio internazionale sulla leishmaniosi canina (LEISHVET) descrivono 4 stadi clinici basati sull'interazione dei risultati sierologici, dei segni clinici, degli esami emato-biochimici ed urinari e suggeriscono il tipo di terapia e l'eventuale prognosi per ognuno di essi (Tab 3). Tabella 1. Stadiazione clinica secondo le linee guida "LEISHVET" (Solano Gallego et al., Parasit & Vectors, 2011, modificato).
Sierologia * Segni Clinici
Di norma non sono Assenza di evidenze
Livelli degli Segni clinici lievi come osservate
Malattia
linfoadenomegalia
clinicopatologiche trattamento.
dermatite papulare
renale alternativa:
Sierologia * Segni Clinici
creatinina < 1.4 antimoniato di n-mg/dl;
non- metilglucamina
proteinurico: UPC miltefosina,
differenti combinazioni**
Anomalie clinicopatologiche
Cani che, oltre ai segni come
possono rigenerativa,
lesioni iperglobulinemia,
o ipoalbuminemia,
solitamente simmetriche
Stadio II bassi
antimoniato di n- Da buona
Malattia medi;
esfoliativa/onicogrifosi, sierica
moderata possibili
ulcere (piano nasale, Sottostadi
anche casi cuscinetti, prominenze a) Profilo renale miltefosina con livelli di ossee,
giunzioni normale:
creatinina < 1.4
anoressia, perdita di mg/dl;
ed proteinurico: UPC
b) Creatinina <1.4 mg/dl; UPC = 0.5-1
Anomalie clinicopatologiche Allopurinolo
Cani che, oltre ai segni elencate
nello antimoniato di n-
elencati negli stadi I e II, stadio
II metilglucamina
Stadio III Livelli
Malattia anticorpi da segni causati dal lesioni
cronica miltefosina
immunocomplessi:
(CKD),stadio 1 IRIS
vasculite, artrite, uveite con UPC > 1 o Seguire le lineeguida
e glomerulonefrite.
stadio 2 (creatinina IRIS per la CKD 1.4-2 mg/dl)
Sierologia * Segni Clinici
Anomalie clinicopatologiche elencate
Cani con i segni clinici stadio
Stadio IV Livelli
elencati nello stadio II. CKD, stadio 3 IRIS Allopurinolo (da solo) Solitamen
Malattia anticorpali Tromboembolismo
da medi ad polmonare, o sindrome mg/dl) e stadio 4 Seguire le lineeguida infausta
uremica e stadio finale IRIS (creatinina > 5 IRIS per CKD della malattia renale
mg/dl) Sindrome uremica: marcata proteinuria UPC > 5
*I cani con livelli anticorpali da medi ad alti dovrebbero essere confermati come infetti attraverso altri metodi diagnostici come citologia, istologia, immunoistochimica o PCR. Alti livelli anticorpali, definiti con un aumento 3-4 volte al di sopra del cut off di un laboratorio accreditato, sono decisivi nella diagnosi di leishmaniosi canina. **Cani nello stadio I (Lieve malattia) richiedono trattamenti meno prolungati con uno o una combinazione di due farmaci o in alternativa monitoraggio e nessun trattamento. Tuttavia, ci sono poche informazioni riguardo questi cani, di conseguenza le opzioni terapeutiche rimangono da definire. Come emerge anche dalle linee guida sopra riportate, uno degli aspetti più importanti da inquadrare in un soggetto leishmaniotico, dal punto di vista clinico, diagnostico, terapeutico e prognostico, è la severità del danno renale. Ciò è possibile attraverso l'impiego della classificazione delle nefropatie croniche stilata dalla International Renal Interest Society (IRIS) (Tab.4). Tabella 2. Stadiazione del paziente nefropatico secondo le linee guida IRIS (2009), modificato da: www.iris-kidney.com Stadio
CREATININA PLASMATICA
A rischio di CKD
Per pazienti identificati come "a rischio" , effettuare controlli regolari e ridurre I fattori di rischio
Presenti alcune altre anomalie renali come inadeguata capacità di concentrazione in assenza di cause non-renali identificabili; riscontri anomali alla palpazione renale e/o alla diagnostica per immagini; proteinuria persistente di origine renale, risultati anormali alla biopsia renale, livelli progressivamente elevati di creatinina
Lieve azotemia renale
La creatinina in questo stadio non sempre è sufficientemente indicativa, in presenza di deficit di escrezione
Azotemia renale moderata
Possono essere presenti segni clinici sistemici
Azotemia renale grave
Sono di solito presenti segni clinici sistemici
Questa classificazione viene ulteriormente perfezionata dalla misurazione della proteinuria (Tab. 5) Tabella 3. Sotto-classificazione IRIS (2009) in relazione al valore della proteinuria (Substage 2a), modificato Valori di UPC
Non-proteinurico (NP)
Proteinurico borderline (BP)
Proteinurico (P)
I pazienti, quando possibile, dovrebbero essere ulteriormente monitorati attraverso la misurazione della pressione sanguigna arteriosa (Tab.6) Tabella 4. Classificazione IRIS (2009): i pazienti sono divisi in sottostadi, in base ai valori della pressione arteriosa Pressione
Sanguigna Pressione
Sanguigna Correzione
quando Sottostadio Pressione
Sistolica (mm Hg)
Diastolica (mm Hg)
sono disponibili I range Arteriosa (AP) di riferimento specifici di razza *
< 10 mmHg al di sopra 0 del range di riferimento Rischio minimo
10-20 mmHg al di sopra 1 del range di riferimento Basso rischio
20-40 mmHg al di sopra 2 del range di riferimento Rischio moderato
≥ 40 mmHg al di sopra 3 del range di riferimento Alto rischio
Nessuna evidenza di complicazioni / danno organico terminale
Nessuna complicazione
Evidenza di complicazioni / danno organico terminale
Pressione sanguigna non misurata
*Se disponibili, è preferibile utilizzare i ranges specifici di razza, come valori normali, e comparare la misurazione con il limite superiore del range per la razza che si st esaminando. I levrieri, in particolare, hanno valori di riferimento più alti della maggior parte delle razze canine. Nel caso di Bella, la misurazione della pressione arteriosa, ha dato un valore medio di 148 mm/Hg. Alla luce del segnalamento, dei dati clinici e di tutti i test di laboratorio eseguiti, Bella è stata classificata in Stadio IV della classificazione LeishVet. Lo stadio IV di malattia purtroppo è il piu' grave e spesso nonostante un repentino e corretto approccio terapeutico la prognosi resta riservata. Ad aggravare la situazione di Bella è inoltre la razza del cane; alcuni studi dimostrano che il Boxer in particolare è geneticamente più predisposto a sviluppare la malattia leishmaniotica. TERAPIA E DISCUSSIONE FINAL2011 Solano-Gallego et al; licensee BioMed Central Ltd. This is an Open Access article distributed under the terms of the Creative Commons Attribution License which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited. Il protocollo diagnostico e terapeutico proposto nel caso di Bella, cui è stato prescritto il ricovero, prevedeva il completamento degli esami ematobiochimici per la messa in evidenza di possibili alterazioni del profilo coagulativo, l'iniziale stabilizzazione del paziente con terapia fluido-elettrolitica per la correzione dell'acidos metabolica, seguita da terapia specifica anti-leishmania (Miltefosine alla dose di 2 mg/kf al giorno per via orale per 28 giorni consecutivi associata ad allopurinolo alla dose di 10 mg/kg due volte al giorno per via orale per diversi mesi) e terapia per il controllo della condizione renale (enalapril, dieta a basso tenore proteico, chelanti del fosforo, antiemetici, eritropoietina). Il cane, ricoverato presso altra struttura per volere del proprietario, è purtroppo deceduto dopo alcuni giorni.
Diagnosi caso 3: E' giallo? C'è un problema!
L'anemia emolitica immunomediata (IMHA) è una delle cause più frequenti di anemia nei piccoli animali. L'IMHA può essere suddivisa in due forme principali: primaria o idiopatica o anemia emolitica autoimmune (AIHA) e secondaria. L'AIHA è un disordine autoimmune la cui origine è e resterà sconosciuta e rappresenta la forma di anemia emolitica più frequente nel cane; l'IMHA secondaria, invece, si verifica in seguito all'instaurarsi di numerosi processi patologici (Tab. 5) Tab.5 Potenziali cause di anemia emolitica immunomediata Farmaci
Trimetoprim/sulfamidici
Levamisolo (cane)
Propiltiouracile (gatto)
FANS (fenilbutazone)
Infezioni/parassiti
Virus della leucemia felina
Emobartonellosi (H. felis nel gatto)
Malattie linfoproliferative (linfoma, leucemie)
Lupus eritematoso sistemico
Reazioni trasfusionali
Isoeritrolisi neonatale (gatto)
antilinfocitaria
L'emoglobinuria è dovuta alla presenza di emoglobina nelle urine che è, a sua volta, indicativa di una intensa emolisi intravasale in atto. L'IMHA è caratterizzata dalla produzione di anticorpi in grado di legarsi alla membrana dei globuli rossi, determinando la riduzione dell'ematocrito o per lisi diretta degli stessi o per rimozione degli eritrociti ad opera del sistema reticolo-endoteliale. In particolare, si parla di emolisi intra- ed extra-vascolare. Nel primo caso, le emazie vengono distrutte in seguito all'adesione dell'anticorpo e del complemento sulla propria superficie; nel secondo caso, invece, dei recettori, localizzati sulla superficie dei macrofagi, aderiscono all'anticorpo attaccato alla superficie eritrocitaria causandone la rottura. L'anemia viene classificata come primaria (idiopatica) quando la causa resta ignota, rappresenta la forma di IMHA più frequente nel cane, colpisce tipicamente in soggetti giovani /adulti, più frequentemente femmine; le razze più colpite sono Cocker spaniel, Springer Spaniel inglese, Barboncino, Bobtail, Pastore scozzese. La forma primaria (AIHA) può essere diagnosticata con assoluta certezza soltanto quando siano state ampiamente valutate le potenziali cause sottostanti. Una ricerca completa di tali cause è però molto difficile, dispendiosa, lunga e spesso infruttuosa. Gli esami di base standard comprendono un esame emocromocitometrico con valutazione dello striscio periferico, un profilo biochimico, esame delle urine, radiografia e/o ecografia addominale. Ulteriori esami da considerare nei pazienti anziani sono volti ad escludere eventuali neoplasie sottostanti ed includono radiografia toracica, ecografia addominale, citologia linfonodale e/o midollare. Nel caso descritto, l'esame clinico del paziente e i risultati delle analisi eseguite hanno permesso di emettere una diagnosi di anemia emolitica immunomediata (IMHA), confermata dalla positività del test di Coombs diretto per la ricerca di anticorpi e/o complemento legati alla membrana eritrocitaria e dall'osservazione microscopica dello striscio di sangue periferico, che ha evidenziato la presenza di sferociti con contemporanea anisocitosi, policromasia, numerosi eritrociti nucleati e, contemporaneamente, ha escluso possibili parassitosi in atto. Gli sferociti sono piccoli eritrociti sferoidali, che si colorano intensamente conservando un pallore centrale. Essi assumono la forma sferoidale in seguito alla riduzione di superficie della membrana cellulare, dovuta alla parziale fagocitosi da parte dei fagociti mononucleati. La presenza di sferociti in un vetrino di sangue periferico indica che gli eritrociti presentano, legati alla loro membrana, anticorpi o complemento che vengono riconosciuti dai recettori espressi sui fagociti. La presenza di sferociti nel cane è un indicatore sensibile di IMHA. Un altro test molto semplice che può essere attuato facilmente nella pratica clinica, qualora si abbia il sospetto di un'anemia emolitica immunomediata, è il test di agglutinazione su vetrino. Esso consiste nel porre una goccia di sangue su di un vetrino: in caso di disordine autoimmune si verificherà un'agglutinazione, ovvero piccoli aggregati di globuli rossi. Se si miscela la stessa goccia di sangue con una di soluzione fisiologica per un paio di minuti, nel caso in cui l'aggregazione non fosse dovuta alla presenza di anticorpi, ci sarà la risoluzione degli stessi; mentre, in caso di disordine autoimmune gli agglutinati persisteranno. Ciò è possibile in quanto talvolta i fenomeni di agglutinazione sono causati dalla presenza di proteine infiammatorie, come il fibrinogeno, che impediscono alle cariche presenti sulla membrana di ogni globulo rosso, di espletare la propria funzione
repulsiva. Una volta effettuata la diluizione ematica con la soluzione fisiologica, però, avviene anche una riduzione della concentrazione delle proteine infiammatorie, per cui i globuli rossi torneranno a separarsi. Nel caso di Maggie anche questa prova ha dato esito positivo. A completamento dell'iter diagnostico sono state escluse patologie concomitanti attraverso test specifici come: ricerca di anticorpi anti-Leishmania infantum ed Ehrlichia canis. Nel caso di Maggie l'iter diagnostico eseguito non ha permesso di riconoscere nessuna delle principali cause di IMHA e, come spesso avviene in questi casi, questo punto rappresenta una vera frustrazione per il veterinario in quanto è improbabile che l'IMHA possa venire efficacemente trattata senza aver identificato la causa scatenante. L'approccio terapeutico in corso di IMHA è duplice: specifico, volto sia alla rimozione della causa scatenante, qualora sia possibile e aspecifico, attraverso terapia sintomatica e di supporto. Nel caso di Maggie, la terapia effettuata è stata solo sintomatica ed ha previsto l'applicazione di un catetere endovenoso, l'attuazione di una fluido terapia con Ringer lattato, l'esecuzione di una trasfusione, data la gravità dell'anemia, terapia immunosoppressiva a base di prednisolone alla dose di 2-4 mg/kg die per via orale fino a normalizzazione dell'ematocrito. Nell'arco di una settimana si è assistito ad un notevole miglioramento delle condizioni cliniche e alla graduale normalizzazione delle analisi di laboratorio. Dopo un mese di terapia immunosoppressiva a dosaggio pieno, l'ematocrito di Maggie ha raggiunto la normalizzazione per cui è stato gradualmente ridotto il dosaggio del prednisolone fino alla sua totale sospensione durante il mese successivo. Maggie ha ottenuto una completa remissione della patologia.
Diagnosi caso 4: Cosa si nasconde dietro il vomito e la diarrea
In seguito ai rilievi clinici e di laboratorio sopra riportati, fu prescritta la seguente terapia: metronidazolo (10 mg/kg, per os, bid), alimentazione a base di z/d ultra (Hill's) per circa un mese. Al controllo successivo, dopo qualche giorno dalla sospensione della terapia, il proprietario riferiva che il paziente durante il trattamento era migliorato ma, subito dopo la sospensione della terapia, la sintomatologia recidivava. Così si decise di sottoporre il soggetto ad una laparotomia esplorativa per individuare, in maniera più specifica, il processo patologico, mediante biopsia ed esame istologico del piccolo intestino. La laparotomia esplorativa ha consentito di localizzare il processo patologico a livello digiunale, mentre i prelievi bioptici hanno permesso di evidenziare, a livello del digiuno, un infiltrato linfoplasmocitico diffuso nei villi intestinali, associato ad aree di sclerosi e ad aspetti di ipersecrezione. Nella parete si osservavano macrofagi, cellule epitelioidi, linfociti e plasmacellule (foto 2). Figura 2 L'esame istologico evidenzia numerose cellule infiammatorie che invadono diffusamente la tonaca muscolare e la sottomucosa e oltrepassano in più punti la muscolaris mucosae infiltrando l'epitelio con scompaginamento dei villi. (Immagine gentilmente concessa dalla Prof.ssa Brunella Restucci – Dipartimento di Medicina Veterinaria e Produzioni Animali)
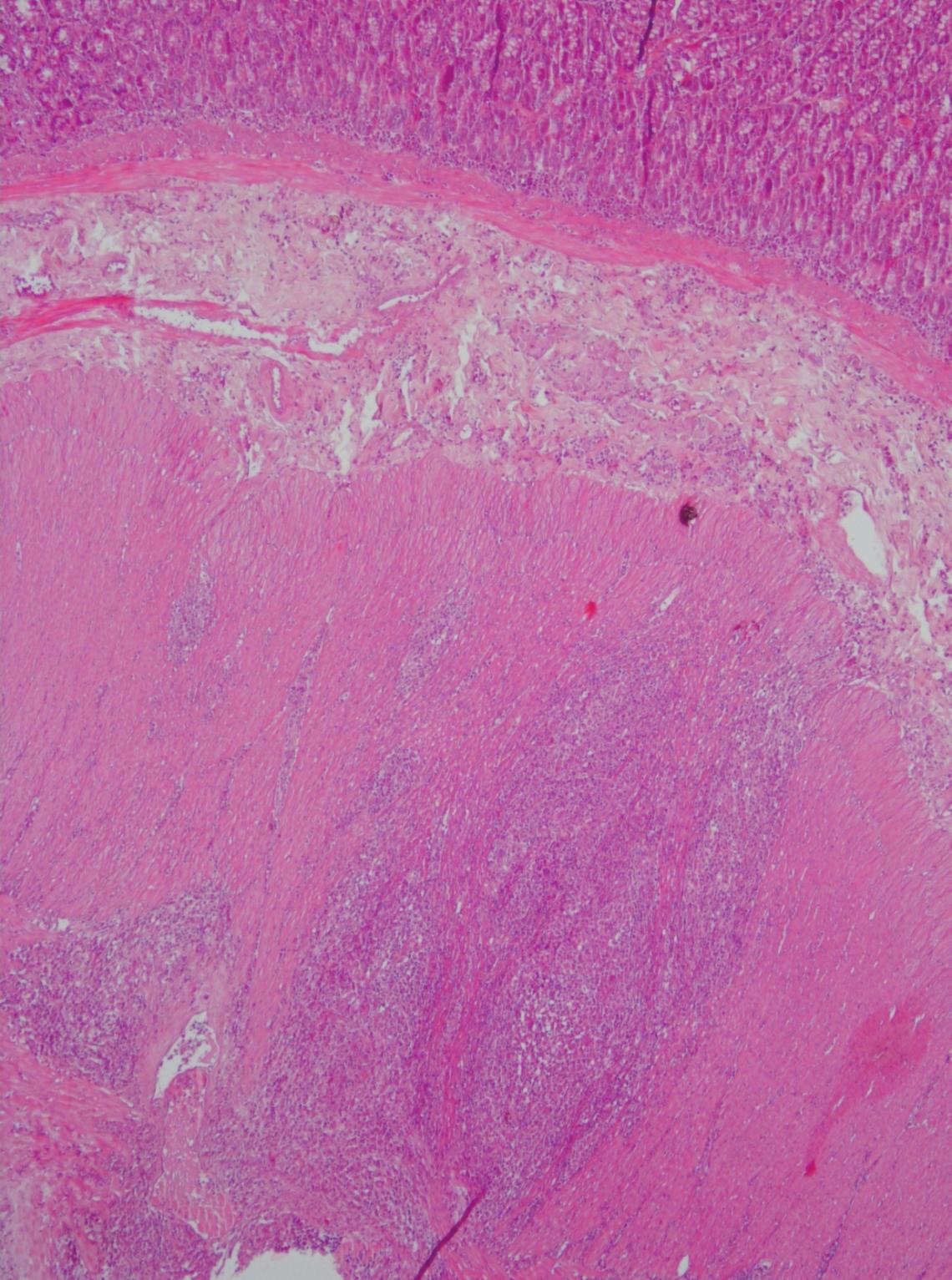
I rilievi clinici, di laboratorio e le indagini collaterali hanno quindi permesso di formulare la diagnosi di enterite granulomatosa proteino-disperdente, ma il raggiungimento tardivo di tale diagnosi non ha consentito l'attuazione di un tempestivo piano terapeutico e la patologia ha avuto un rapido esito infausto. L'enterite granulomatosa del cane è una rara forma di IBD, ad andamento cronico, poco riportata in letteratura veterinaria sia nel cane che negli altri animali domestici. Si caratterizza per una flogosi granulomatosa transmurale che coinvolge con più frequenza l'ileo distale e la giunzione ileo-colica causando un ispessimento e una stenosi di questa regione; può tuttavia interessare anche lo stomaco, il duodeno, il retto ed i linfonodi regionali. La malattia colpisce con maggiore frequenza cani di sesso maschile intorno ai 4-5 anni di età. Dal punto di vista clinico l'enterite granulomatosa è responsabile di diarrea cronica abbondante ed acquosa, mista a sangue e/o muco, perdita di peso, anoressia, occasionalmente vomito violento ed emorragico, costipazione in caso di stenosi intestinale per le lesioni granulomatose. Alla palpazione addominale è possibile rilevare un ispessimento delle anse intestinali, e nel caso in cui il
processo patologico interessi anche il retto, all'esplorazione rettale si può rilevare stenosi ed ispessimento della mucosa. La localizzazione rettale delle lesioni può esitare nella formazione di fistole perianali. I rilievi di laboratorio nella maggior parte dei casi mostrano un ipoproteinemia ed una lieve o moderata eosinofilia. L'esame radiografico con mezzo di contrasto evidenzia le ulcerazioni ed i restringimenti irregolari del lume intestinale, ma la diagnosi deve essere ulteriormente confermata da un esame endoscopico ed istopatologico di tessuto prelevato mediante biopsia. All'esame endoscopico la superficie mucosa colpita appare iperemica, granulosa, ulcerata ed ispessita. Le lesioni granulomatose hanno istologicamente un aspetto polimorfo per la presenza di linfociti, plasmacellule e soprattutto eosinofili. Oltre alle lesioni focali si può riscontrare un'infiammazione mista e diffusa a carico della lamina propria delle porzioni intestinali adiacenti, apparendo anch'esse ispessite ed infiammate. L'eziopatogenesi dell'enterite regionale, come delle altre forme di IBD, è sconosciuta, inoltre l'estrema rarità dei casi finora descritti rende ancora più difficile la formulazione di ipotesi eziopatogenetiche. Diverse indagini svolte per la ricerca di specifici agenti infettivi (Histoplasma capsulatum, Prototheca spp., micobatteri, tricocefali) , responsabili di flogosi granulomatose transmurali, sono risultate negative, supportando cosi la natura idiopatica della patologia. Maggiori difficoltà si incontrano nella differenziazione della malattia tubercolare in quanto il granuloma è composto da cellule epitelioidi ed è difficile evidenziare i micobatteri, rare sono le cellule giganti, alla periferia del granuloma la componente linfo-plasmocitaria è ben rappresentata ed il riscontro di granulociti neutrofili non è frequente. L'interesse per queste rare forme di enteriti granulomatose di tipo idiopatico del cane si è notevolmente accresciuto negli ultimi anni, per le molteplici analogie con il morbo di Crohn dell'uomo. Il morbo di Crohn è una delle due forme di IBD dell'uomo, accanto alla colite ulcerosa. E' un processo infiammatorio transmurale che può interessare qualsiasi tratto del canale alimentare, dalle labbra al margine anale, anche se la forma ileo-colica resta il quadro più comune di comparsa. Il morbo di Crohn colpisce i due sessi indifferentemente, l'età di comparsa della malattia abbraccia la fascia dai 20 ai 40 anni, ma sono descritti anche diversi casi in bambini ed anziani. La malattia presenta una distribuzione segmentale, interessa cioè tratti d'intestino intervallati da aree apparentemente normali. Il morbo di Crohn resta una patologia idiopatica la cui eziopatogenesi è ancora affidata a numerose ipotesi che ricalcano in parte le differenti teorie già riportate per la genesi delle IBD del cane. La grande variabilità del decorso clinico del morbo di Crohn rende difficoltosa la valutazione di protocolli terapeutici. Pur in assenza di una precisa definizione eziopatogenetica, il riconoscimento del coinvolgimento del sistema immunitario nella genesi di queste enteropatie infiammatorie croniche, ha reso possibile e vantaggioso l'impiego nell'uomo degli antinfiammatori steroidei e non e di farmaci immunosoppressori. Per quanto riguarda l'enterite regionale del cane, i pochi casi riportati e la gravità degli stessi, non permettono di stabilire un preciso protocollo terapeutico. Il trattamento con prednisolone, sulfasalazina, tilosina, porta solo remissioni temporanee della malattia. Anche la resezione chirurgica delle lesioni granulomatose segmentarie non esclude la possibilità di recidive nel tempo o un buon recupero funzionale. Non per ultime, le modifiche all'alimentazione, rappresentano un ottimo ausilio terapeutico in corso di patologie intestinali croniche. E' doveroso sottolineare che l'enterite regionale del cane e il morbo di Crohn, sebbene presentino diverse analogie dal punto di vista anatomo-patologico, non sono identiche. Il caso clinico descritto testimonia la rarità della patologia riscontrata, inoltre conferma che risulta una patologia insidiosa dal punto di vita diagnostico, manifestandosi con segni clinici e alterazioni ematobiochimiche aspecifiche: solo il ricorso all'esame istologico dei campioni bioptici ha consentito di emettere una diagnosi definitiva, ma il raggiungimento della stessa è avvenuto troppo tardivamente rispetto alla progressione della patologia, con conseguente morte del paziente. Lo studio del caso clinico di
Astra ha inoltre confermato la difficoltà nel determinare l'eziopatogenesi dell'enterite granulomatosa, o quanto meno i fattori predisponenti la stessa. Diagnosi caso 5: Poldo è molto stanco, è malato? La diagnosi di certezza è stata ottenuta attraverso la valutazione della funzionalità della tiroide misurando la concentrazione sierica basale della tiroxina (T4) e del TSH endogeno specifici per la specie canina. (Tabella 2) Tabella 5 Esplorazione della funzionalità tiroidea di Poldo
T4 (totale canino)
0.03 – 0.45 g/dl
In seguito ai rilievi clinici e di laboratorio sopra riportati è stata, quindi, confermata la diagnosi di ipotiroidismo e prescritta la seguente terapia: levotiroxina sodica (T4 sintetico) (0.02 mg/kg per per os, bid) a stomaco vuoto. La levotiroxina sintetica è la molecola d'elezione per il trattamento dell'ipotiroidismo. La somministrazione per via orale dovrebbe normalizzare le concentrazioni sieriche di T4, T3 e di TSH, testimoniando che questi prodotti possono essere convertiti dai tessuti periferici in T3 metabolicamente più attivo. La dose di partenza è di 0.02 mg/kg di peso corporeo ogni 12 ore. Il dosaggio iniziale e la frequenza delle somministrazioni sono solo il principio, poiché a causa della variabilità dell'assorbimento e del metabolismo della maggior parte dei cani, i valori indicati potranno richiedere delle correzioni prima di poter osservare una risposta clinica completa. L'integrazione con ormone tiroideo andrebbe, quindi, continuata minimo per un periodo di 4-8 settimane prima di poter stimare l'efficacia del trattamento che si valuterà attraverso la regressione dei segni clinici e della alterazioni clinico-patologiche. Durante i primi 10 giorni di trattamento Poldo è diventato più vigile e attento agli stimoli esterni, questo fatto rappresenta un indicatore precoce ed importante che conferma la diagnosi di ipotiroidismo. Nel mese successivo ha presentato anche una ricrescita del pelo. Poldo è ancora sotto osservazione in quanto la risoluzione completa della sintomatologia solitamente richiede almeno 3-6 mesi.
Diagnosi caso 6: L'aumento di volume dei linfonodi è un sintomo da non sottovalutare
La diagnosi di certezza è stata ottenuta attraverso l'esame citologico linfonodale che ha confermato che Arash è affetto da linfoma a grandi cellule. Il linfoma, rappresenta una delle principali neoplasie riscontrabili nel cane e nel gatto, esso è definito come una proliferazione di cellule linfoidi maligne a carico principalmente di linfonodi, fegato e milza. Dal punto di vista eziologico, l'origine di tale neoplasia è sconosciuta, sebbene nel gatto alcune varietà di linfoma siano state correlate ai virus dell'immunodeficienza felina (FIV) e della leucemia felina (FeLV).Si tratta di una patologia che coinvolge principalmente soggetti di mezza età o anziani (6-12 anni) ma può riscontrarsi anche in soggetti più giovani. Nel cane, è presente una evidente predisposizione di razza, come ad esempio nel caso di Boxer, Basset Hound, Rottweiler, Cocker Spaniel, Golden Retriever, San Bernardo, Bulldog Inglese. In base alla forma anatomica assunta, il linfoma può essere distinto in:
Linfoma multicentrico: forma più comune nel cane, caratterizzata da linfoadenomegalia generalizzata, con linfonodi periferici aumentati di volume ma non dolenti, che in genere trae origine dai linfonodi sottomandibolari e prescapolari e successivamente coinvolge gli altri oltre a interessare fegato, milza e/o midollo osseo. E' possibile riscontrare altri segni clinici, aspecifici, come perdita di peso, anoressia, letargia, poliuria e polidipsia, episodi febbrili. Linfoma alimentare: forma meno frequente, che si manifesta con segni clinici specifici del tratto gastroenterico, come vomito e diarrea, perdita di peso, inappetenza, malassorbimento, ipoproteinemia. Si manifesta con un'infiltrazione multifocale o diffusa del tratto gastroeneterico, in presenza o meno di linfoadenomegalia endoaddominale. Linfoma mediastinico: si tratta di una forma rara, caratterizzata dall'aumento di volume dei linfonodi mediastinici e/o infiltrazione del midollo osseo, con conseguente sviluppo di segni clinici come dispnea,tosse, rigurgito, intolleranza all'esercizio fisico, alterazioni del ritmo cardiaco. Spesso si accompagna allo sviluppo di ipercalcemia, di conseguenza sono riscontrabili anche poliuria e polidipsia. Linfoma extranodale: può colpire qualsiasi distretto anatomico, con conseguente sintomatologia estremamente variabile a seconda dell'organo interessato (linfoma cutaneo, oculare, renale, encefalico, cardiaco, osseo, nasale, endocrino, muscolare, polmonare, faringeo, vescicale, uretrale e prostatico). In corso di linfoma, la sintomatologia riscontrata può ulteriormente essere aggravata dalla comparsa di eventuali sindromi paraneoplastiche che spesso si associano a tale tipo di neoplasia. Le sindromi paraneoplastiche sono secondarie alla sintesi e alla liberazione di sostanze biologicamente attive, come ormoni, fattori di crescita e citochine: a seconda dell'organo bersaglio, esse possono essere classificate in disordini generali, ematologici, cutanei, neuromuscolari ed endocrini (Tabella 3). Tabella 3. Sindromi paraneoplastiche descritte negli animali domestici. SINDROMI PARANEOPLASTICHE
MANIFESTAZIONI GENERALI:
MANIFESTAZIONI EMATOLOGICHE:
Anoressia/cachessia tumorale
MANIFESTAZIONI ENDOCRINE:
Ipercalcemia maligna
MANIFESTAZIONI CUTANEE:
Iperaggregabilità piastrinica
Dermatite necrolitica superficiale
Dermatofibrosi nodulare
Disturbi dell'emostasi
MANIFESTAZIONI NEUROMUSCOLARI:
Miastenia gravis
MANIFESTAZIONI GASTROENTERICHE:
Neuropatia periferica
Ulcere gastroduodenali
Oltre a quella anatomica, per una migliore caratterizzazione istologica e/o stadiazione dei linfomi, nel corso degli anni sono state sviluppate diverse classificazioni, come quella della World Health Organization (WHO) o quella di Kiel, le più famose, ed altre sono ad oggi in via di sviluppo. Data l'estrema variabilità della sintomatologia clinica, in corso di linfoma la diagnosi di certezza richiede sempre un approfondimento diagnostico, che prevede indagini aspecifiche, come quelle emato biochimiche, urinarie, ecografiche e radiografiche, e indagini specifiche ovvero esami citologici e istopatologici. Nel caso di Arash, in seguito ai rilievi clinici, di laboratorio ed ecografici, è stato possibile classificare la patologia come linfoma multicentrico al IV stadio clinico, sottostadio b,secondo la classificazione WHO (Tabella 4). Tabella 4. Stadiazione clinica del linfoma degli animali domestici, secondo la World Health Organization.
Linfonodo singolo
Linfonodi multipli in area regionale
Linfoadenopatia generalizzata
Coinvolgimento di fegato e/o milza (con o senza stadio III)
Coinvolgimento di midollo osseo o sangue e/o di qualsiasi organo non linfoide (con o senza stadi da I a IV)
Assenza di segni clinici di malattia
Presenza di segni clinici di malattia
L'esame citologico del sangue periferico ha infatti escluso la presenza di cellule neoplastiche in circolo. Questo dato è stata ulteriormente confermato dall'esame citologico del midollo osseo che ha escluso metastasi in questa sede. La prognosi in questi casi è sempre riservata. Scegliere di sottoporre il proprio animale a chemioterapia è quindi una decisione molto difficile. Il compito del veterinario è inizialmente consigliare il protocollo chemioterapico più indicato per il tipo di neoplasia diagnosticata e, soprattutto, in relazione alle condizioni fisiche del paziente, le aspettative del proprietario, degli effetti collaterali e delle possibili complicazioni. Il medico veterinario è inoltre tenuto a illustrare tutti i rischi associati alla somministrazione dei farmaci antineoplastici da parte del veterinario ed alla convivenza tra animale sottoposto a chemioterapia e le persone che vivono con lui; il sangue e tutti gli escreti e secreti degli animali trattati (urine, feci, saliva, lacrime e vomito) sono una potenziale fonte di contaminazione per un tempo variabile in base ai farmaci impiegati, per cui durante l'intero trattamento si devono utilizzare tutte
le apposite misure di sicurezza per la loro manipolazione così come per il materiale potenzialmente contaminato. I protocolli terapeutici sono numerosi ed in continua evoluzione anche in relazione alla comparsa di nuovi farmaci. L'elenco dei protocolli più impiegati (Tabella 4) è quindi solo indicativo e non esaustivo. Tabella 4. Principali protocolli di trattamento per il linfoma del cane 1) Protocollo "Wisconsis", University of Wisconsis-madison School of Veterinary Medicine
di Principio attivo
somministarzione
1.5 mg/kg PO q24h
1.0 mg/kg PO q24h
0.5 mg/kg PO q24h
di Principio attivo
somministrazione
Ogni 12 h per 7 Prednisone
giorni, poi ogni 24 h per 5 settimane
Giorno: 4, 5, 6, 7 di Ciclofosfamide
ciascuna settimana di trattamento
Fase di mantenimento
Giorno: 4,5,6,7, di Ciclofosfamide
ciascuna settimana
Fase di induzione
di Principio attivo
somministrazione
ciascuna settimana di trattamento
Fase di mantenimento
Dopo il giorno 63 della fase di induzione, ripetere ogni 21 giorni il trattamento
4) Monoterapia con Doxorubicina
Fase induzione (9 settimane)
di Principio attivo
somministrazione
Ogni 21 giorni per Doxorubicina
superare la dose massima cumulativa di 250 mg/m2)
Fase di mantenimento
Non esiste. Dopo l'induzione della remissione il soggetto va monitorato periodicamente, nel caso di recidiva si ripete lo stesso protocollo per un massimo di 8 trattamenti o si passa al COP
Fase di induzione
di Principio attivo
somministrazione
Settimana: 1,2,3,7 Vincristina
Settimana 7 e 12 Ciclofosfamide
somministrazioni)
Settimana 7,8 e 9
10.000 UI/m2 SC o IM
Tutti i giorni la Prednisone
prima settimana , poi a giorni alterni fino alla settimana 12, poi scalare fino alla settimana 15
Fase di mantenimento
In caso di recidiva almeno 4 mesi dopo l'ultima settimana di induzione, ricominciare il protocollo. Se la recidiva è più precoce scegliere altro protocollo.
Tutti i trattamenti si sospendono dopo venticinque settimane in caso di completa remissione della sintomatologia. Prima di ogni seduta chemioterapica deve essere eseguito un esame emocromocitometrico completo con formula leucocitaria in quanto, qualora la conta dei granulociti neutrofili fosse <2.000/ml, il protocollo va sospeso fino al ripristino della normalità e vanno affrontate in modo repentino le possibili complicanze legate alla grave neutropenia. Arash è stato sottoposto a chemioterapia con protocollo Madison-Wisconsis. Dopo le prime 3 settimane di trattamento, Arash presentava ancora una condizione clinica molto grave, continuava a perdere peso nonostante si alimentasse regolarmente, alla palpazione i linfonodi risultavano ancora notevolmente aumentati di volume e l'esame emocromocitometrico evidenziava una grave neutropenia (1600 neutrofili/ml). Tutto ciò ha imposto la sospensione del protocollo chemioterapico ed un trattamento a base di fattore ricombinante metioninico stimolante le colonie granulocitarie (G-CSF) (filgrastim 5 g/kg ogni 24 ore, SC, ad effetto) in attesa di poter riprendere la terapia specifica. Dopo circa 10 giorni di sospensione l'esame emocromocitometrico di controllo mostrava la normalizzazione dei valori di riferimento dei leucociti e quindi è stato ripreso il trattamento chemioterapico. I controlli clinici ed ematologici successivi hanno evidenziato una costante remissione della sintomatologia del paziente (riduzione di volume dei linfonodi esplorabili, aumento di peso, maggiore vitalità) e l'esame emocromocitometrico presentava la normalizzazione di tutte le popolazioni cellulari. Ad oggi Arash è ancora sottoposto a trattamento chemioterapico e continua a rispondere positivamente alla terapia.
Diagnosi caso 7:Mai fermarsi all'apparenza! Considerata l'anamnesi, la sintomatologia clinica e i risultati ottenuti dalle varie indagini collaterali, la principale diagnosi di sospetto formulata è stata quella di ipoadrenocorticismo primario (morbo di Addison); di conseguenza come ulteriore approfondimento diagnostico è stato effettuato il test di stimolo con ACTH (Tabella 6). Tabella 2. Risultati del test di stimolo con ACTH
TEST DI STIMOLO CON ACTH
VALORI DI RIFERIMENTO
CORTISOLO DOPO 90' DALLA
SOMMINISTRAZIONE DI ACTH
L'esecuzione del test di stimolazione con ACTH è risultata decisiva nel confermare il sospetto diagnostico formulato. Il morbo di Addison, o ipoadrenocorticismo primario, è una malattia endocrina caratterizzata da una deficiente produzione di ormoni mineralcorticoidi e glicocorticoidi da parte della ghiandola surrenale, in genere imputabile alla distruzione dell'85-90% della corticale surrenale, in seguito a danno di origine immunomediata; altre cause, più rare, possono essere neoplasie, amiloidosi, traumi, coagulopatie e malattie micotiche. L'ipoadrenocorticismo può più raramente essere secondario, ovvero conseguente ad una ridotta produzione di ACTH da parte dell'ipofisi secondaria a neoplasie, trauma cranico o infiammazione; in questo caso si manifesterà un'atrofia dei corticosurreni e insufficiente produzione di glucocorticoidi, ma non di mineralcorticoidi. Infine, l'ipoadrenocorticismo può essere di origine iatrogena, secondario a somministrazione di farmaci o interventi chirurgici. L'ipoadrenocorticismo primario, può colpire cani e gatti di qualsiasi età, ma più facilmente è riscontrato in soggetti di età compresa tra 4-6 anni, con una maggiore incidenza nelle femmine non sterilizzate; nel gatto non esiste particolare predisposizione di razza mentre nel cane possono essere più colpiti: Cane d'acqua Portoghese, West Highland White Terrier, Border Collie, Rottweiller, Springer Spaniel, Bassett Hounds, Leonberger. La sintomatologia clinica, in corso di Addison, è estremamente aspecifica con insorgenza spesso insidiosa e comprende manifestazioni gastrointestinali, perdita di peso, inappetenza/disoressia, abbattimento del sensorio,debolezza, dolorabilità addominale, poliuria e polidipsia, tremori; tale sintomatologia può acutizzarsi quando l'animale è sottoposto a stress. Alla visita clinica di un soggetto affetto da morbo di Addison, è possibile riscontrare: disidratazione, tempo di riempimento capillare rallentato, polso debole, bradicardia e bradisfigmia, dolorabilità alla palpazione dell'addome. Nei casi più gravi, il soggetto è in stato di shock ipovolemico (crisi addisoniana): l'animale viene trovato in uno stato di collasso, ha polso debole, bradicardia, ipotermia e grave disidratazione. Una crisi addisoniana andrebbe sempre considerata nella diagnosi differenziale di soggetti in stato di shock ipovolemico da cause sconosciute che presentino concomitante bradicardia, in quanto quest'ultima è una risposta inappropriata nei soggetti collassati e ipovolemici.
Le alterazioni più evidenti che si possono riscontrare in seguito all'esecuzione delle indagini di laboratorio sono: Esame emocromocitometrico: di norma è possibile riscontrare una lieve anemia normocitica normocromica, tuttavia, spesso tale condizione risulta mascherata dall'emoconcentrazione conseguente ad un grave stadio di disidratazione; i globuli bianchi possono essere normali, aumentati o ridotti, e nella conta leucocitaria in genere è possibile riscontrare eosinofilia e linfocitosi. Profilo biochimico: sono riportati aumento delle transaminasi, leggera ipoglicemia, ipoalbuminemia, aumento di urea e creatinina, iperfosfatemia, ipercalcemia. Iponatremia, ipocloremia, iperkaliemia: sono le alterazioni più tipicamente riscontrabili, secondarie alla carenza dell'ormone mineralcorticoide, l'aldosterone, normalmente responsabile del riassorbimento a livello renale di sodio, cloro e acqua e dell'eliminazione del potassio. L'incapacità di trattenere sodio e cloro causa la riduzione di volume dei liquidi extracellulari, con conseguente ipovolemia, ipotensione, riduzione della gittata cardiaca e diminuita perfusione di reni e altri tessuti. La mancata escrezione di potassio e, quindi, l'aumento della quota circolante si ripercuote particolarmente a livello cardiaco con riduzione dell'eccitabilità cardiaca, rallentamento della conduzione e prolungamento della fase di refrattarietà del miocardio. Di norma, in un soggetto sano, il rapporto tra sodio e potassio risulta compreso tra 27:1 e 40:1, mentre nei soggetti con ipoadrenocorticismo primario, esso è al di sotto di 27:1 e in casi più gravi di 20:1. Nonostante l'iponatremia, l'ipocloremia e l'iperkaliemia siano dei reperti frequenti, è importante considerare che essi non sono patognomonici di morbo di Addison, ma possono presentarsi in numerose condizioni patologiche, così come non necessariamente un soggetto affetto da ipoadrenocorticismo primario può manifestare tali alterazioni. Esame delle urine: in genere un aumento compensatorio nel peso specifico delle urine (PS> 1030) dovrebbe consentire la differenziazione tra l'iperazotemia prerenale e quella primaria renale (e quindi la diagnosi differenziale con l' insufficienza renale); tuttavia in molti cani affetti da Addison è presente una ridotta capacità di concentrare l'urina (PS <1030). Acidosi metabolica: la ridotta concentrazione di aldosterone fa si che non vengano eliminati idrogenioni a livello renale, ciò, in associazione all'ipovolemia, l'ipotensione e l'ipoperfusione, porta allo sviluppo di acidosi metabolica. Tutte le alterazioni sopra riportate, possono solo aiutare a formulare un sospetto diagnostico in corso di Addison ma, per avere una diagnosi di certezza, sono indispensabili ulteriori approfondimenti ed, in particolar modo, il test d'elezione è rappresentato dal test di stimolazione con ACTH. L'esame radiografico, ecografico e una valutazione elettrocardiografia del cuore, solo altresì delle indagini che andrebbero sempre comprese nel pannello diagnostico. La terapia, nei soggetti che manifestino condizioni gravi e acute come quelle di Filippo, deve essere volta a eliminare l'ipotensione, l'ipovolemia, gli squilibri elettrolitici, l'acidosi metabolica, a favorire la circolazione e fornire i glucocorticoidi. Essa quindi si avvale di: Fluidoterapia endovenosa: somministrare NaCl 0,9% alla velocità di 60-90 ml/kh/h per le prime due ore, successivamente regolare la velocità di infusione a seconda dei parametri vitali del paziente. In genere, una corretta fluidoterapia rappresenta l'elemento cardine nella ripresa del paziente, contribuendo sia a ridurre
lo stato di ipovolemia e ipoperfusione, correggere iponatremia e ipocloremia, ma soprattutto essa può risultare decisiva nella risoluzione dell'iperkaliemia, grazie alla diluizione della quota ematica di potassio e stimolandone l'eliminazione renale. La terapia endovenosa può prevedere anche l'aggiunta di soluzioni di Glucosio 5% , per trattare un'eventuale ipoglicemia riscontrata. Correzione dell'iperkaliemia: più raramente l'iperkaliemia richiede uno specifico trattamento, in questo caso può essere utile la somministrazione di 0,2 UI/kg di insulina seguita da un bolo di glucosio, e l'aggiunta di soluzione a base di Glucosio 5% alla terapia endovenosa. Nei casi più gravi, è possibile somministrare calcio gluconato 10% (0,5-1,5 ml/kg ev ogni 15-20 minuti), che ha un'azione cardioprotettiva, antagonizzando gli effetti dell'ipekaliemia a livello dei potenziali di membrana. Correzione dell'acidosi metabolica: in genere i soggetti affetti da Addison presentano una modesta acidosi metabolica che non richiede un intervento terapeutico, in quanto la corretta reidratazione, con la riperfusione tissutale e l'incremento della velocità di filtrazione glomerulare, risulta sufficiente. Nei casi particolarmente gravi, in cui sia riscontrata una persistente e grave acidosi metabolica (ph < 7,1 o HCO3 < 12 mmol/l) occorre intervenire con la somministrazione di bicarbonato, il cui deficit può essere calcolato come: 0,3 x peso corporeo (kg) x (HCO3 ideale – HCO3 del paziente). Della quota ottenuta, ¼ deve essere somministrato tra le 6-8 ore e poi andrebbe rivalutato l'equilibrio acido-base del paziente. Anche la terapia con sodio bicarbonato contribuisce a risolvere l'iperkaliemia. Integrazione di glucocorticoidi: nella fase della crisi addisoniana, dovrebbe essere iniettato un glucocorticoide a rapida azione, come idrocortisone (2-4 mg/kg ev), o prednisolone sodio succinato (4-20 mg/kg ev). Idealmente, il test di soppressione con ACTH andrebbe eseguito sempre prima della somministrazione dei glucocorticoidi, in quanto sia idrocortisone che prednisone vengono misurati insieme al cortisolo endogeno, interferendo con la corretta esecuzione del test. Se non è possibile, alternativa è la somministrazione di desametasone sodio fosfato (0,5-4 mg/kg ev). Integrazione di mineralcorticoidi: i prodotti ad oggi disponibili sono il desossicorticosterone pivalato (DOCP) al dosaggio di 2,2 mg/kg im ogni 25 giorni, oppure il fludrocortisone acetato (0,02 mg/kg) somministrato per via orale o endorettale.
Terapia sintomatica: il vomito o la nausea possono essere trattati con farmaci antiemetici o gastroprotettori; l'anemia, se particolarmente grave, può richiedere una trasfusione di sangue; se le condizioni lo richiedono può rendersi necessaria una copertura con antibiotici ad ampio spettro. Nella maggior parte dei pazienti trattati in maniera corretta, sia i valori degli elettroliti, che le altre alterazioni ematologiche, rientrano nell'arco di 24-48 ore; in ogni caso i soggetti andrebbero comunque monitorati per alcuni giorni, in quanto, anche se raramente, potrebbero insorgere alcune complicanze, come sepsi, insufficienza renale acuta o DIC. Nel caso di Filippo, la terapia è risultata decisiva nel superamento della crisi e la maggior parte delle anomalie riscontrate alla prima visita già dopo 24h sono rientrate (figura 3 ). Figura 3. Emogas su sangue venoso dopo 24 h
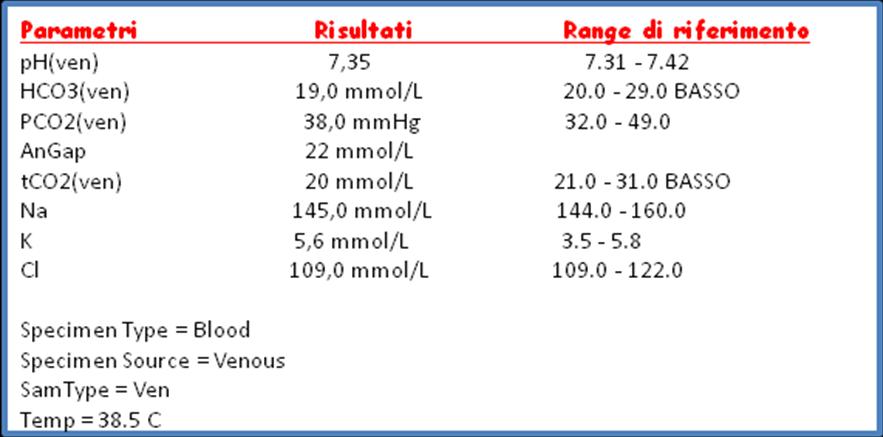
Dopo una settimana di ricovero, Filippo è stato dimesso con la terapia di mantenimento, che in genere prevede: Glucocorticoidi : prednisone ad un dosaggio iniziale di 0,22 mg/kg bid; Mineralcorticoidi: DOCP al dosaggio di 2,2 mg/kg im ogni 25 giorni oppure fludrocortisone (0,02 mg/kg PO bid o sid) . Il fludrocortisone è dotato di una significativa attività glucocorticoide, meno del 50% dei pazienti trattati con esso richiede l'ulteriore aggiunta di prednisone alla terapia.
Diagnosi caso 8: Perché il cane si gratta?
Ambra è stata portata a visita dopo un mese di dieta ed ha mostrato una completa guarigione: assenza di prurito e scomparsa delle lesioni cutanee e dell'otite esterna. E' stata quindi formulata la diagnosi si allergia alimentare. Cani e gatti possono sviluppare reazioni avverse al cibo su base immunologica (allergia propriamente detta) o non immunologica (intolleranza). L'intolleranza a sua volta può essere dovuta a : reazioni idiosincrasiche: dovute alla de granulazione aspecifica dei mastociti a causa di fattori rilascianti l'istamina o all'istamina contenuta in alcuni alimenti; reazioni metaboliche: dovute all'incapacità del soggetto di digerire alcuni componenti della dieta (es. lattosio); reazioni farmacologiche: dovute all'effetto farmacologico di alcune sostanze contenute nel cibo (xantine nel cioccolato); reazioni tossiche: dovute a tossine presenti nel cibo o prodotte da batteri (es. botulino) o micotossine presenti nell'alimento. L'allergia alimentare rappresenta il 10-15 % delle patologie cutanee su base allergica, non sembra presentare una predisposizione di razza o di sesso e si manifesta in età inferiore ai sei mesi – un anno. Se la reazione è di natura immunologica l'animale deve venire a contatto più volte con lo stesso alimento prima che si sensibilizzi. L'alimento all'interno del tubo gastroenterico incontra una serie di difese che impediscono che proteine estranee entrino in contatto con l'organismo (enzimi pancreatici, enterociti, IgA secretorie e circolanti, cellule mononucleari-fagocitarie del sistema linfoide associato al fegato e
all'intestino). E' possibile che, quando la mucosa intestinale è danneggiata, per esempio a causa di parassiti o virus, la barriera protettiva locale non sia in grado di bloccare il passaggio di proteine del cibo a livello sistemico, provocando una risposta allergica anche in organi lontani come la cute. E' probabile che anche lo svezzamento precoce possa causare l'alterazione della barriera protettiva locale, così come gravi infestazioni parassitarie intestinali. Alla base del meccanismo immunologico responsabile dell'allergia alimentare si pensa che sia predominante una reazione di ipersensibilità di tipo I e in secondo luogo di tipo III e IV. Le reazioni di tipo I sarebbero responsabili del prurito, mentre quelle di tipo III potrebbero causare segni intestinali acuti (diarrea), osservabili a volte in alcuni soggetti. Reazioni di tipo IV, invece, sono probabilmente responsabili della persistenza del prurito anche per lungo tempo dopo l'assunzione dell'alimento che lo ha scatenato. Gli antigeni in causa sono solitamente proteine ad alto peso molecolare (lipoproteine, lipoproteine) in genere 18-36 kD. Gli antigeni possono essere stabili alla cottura e alla digestione. La carne bovina ed i latticini sono responsabili del 40-80% delle reazioni allergiche nel cane ed andrebbero testati per primi; seguono: cereali, granaglie, maiale, pollame, soia, uova, pesce. Il quadro clinico è caratterizzato dal coinvolgimento principalmente della cute (85-90%) e dell'apparato gastroenterico (10-15%), più raramente sono descritti sintomi quali asma, cistiti e crisi epilettiche. Il prurito è il sintomo principale, può comparire entro 4-24 ore dall'ingestione dell'allergene o dopo più tempo e persistere durante tutta la giornata. Si localizza su: zampe, ascelle, inguine, aree periorbitali, muso, orecchie (80% dei soggetti può presentare otite). Le lesioni dermatologiche primarie sono le papule associate a lesioni secondarie come escoriazioni, croste, eritema, seborrea, iperpigmnetazione, piodermite secondaria e infezione da malassezia. La diagnosi differenziale va fatta con tutte le patologie cutanee accompagnate da prurito (vedi tab. 1). La diagnosi si ottiene, come nel caso di Ambra, in seguito a risposta positiva al cambio di dieta ed è confermata dalla provocazione con il vecchio cibo; se il prurito recidiva dopo 1-10 giorni di somministrazione della vecchia dieta il test di provocazione si considera positivo. Se il proprietario vuole ed è disponibile si può individuare l'allergene responsabile della reazione, inserendo uno alla volta, a distanza di una settimana, i componenti della vecchia dieta sino a riottenere la reazione allergica. Normalmente sono solo uno o due componenti della dieta a causare l'allergia, raramente sono coinvolti 3-5 allergeni. I proprietari di Ambra per il momento hanno deciso di non sottoporla alla prova di provocazione.
Diagnosi caso 9: Il sovrappeso non è sinonimo di buona salute!
Considerando il segnalamento, l'anamnesi e i riscontri alla visita clinica, ma soprattutto i risultati ottenuti
dalle indagini di laboratorio, la diagnosi formulata è stata quella di diabete mellito.
è una delle endocrinopatie più frequenti nel cane e del gatto (incidenza dello 0,5%), esso
consiste in un'iperglicemia derivante da un deficit di secrezione e/o di azione dell'insulina.
In Medicina Veterinaria, viene suddiviso in:
di tipo 1: è la forma più comune nel cane ed è caratterizzato da una distruzione completa
delle cellule β con progressiva ed assoluta carenza insulinica. L'eziologia è tutt'ora poco nota, sebbene siano
stati identificati come fattori la predisposizione genetica, diete eccessivamente ricche di carboidrati,
meccanismi immunomediati e fattori ambientali.
di tipo 2: risulta essere la forma più frequente nel gatto (80-95% dei gatti diabetici).
Anch'esso ha alla base un'eziologia complessa che prevede una combinazione di fattori genetici ed
ambientali, inoltre il rischio aumenta con l'avanzare dell'età. Alla base di questa forma di c'è
un'insulinoresistenza che può riconoscere diverse cause tra cui obesità, livelli elevati di ormone della
crescita, cortisolo, progesterone. L'iperglicemia derivante dall'insulinoresistenza stimola le cellule β
pancreatiche a produrre maggiori quantità di insulina, finchè quest'ultima non risulta più sufficiente per
soddisfare la domanda; la conseguente iperglicemia, riduce ulteriormente la capacità delle cellule β di
rispondere all'insulina da glucosio) fino ad arrivare a un completo esaurimento della funzionalità
delle stesse. Spesso a questo tipo di diabete è associata una pancreatite che porta alla perdita di
funzionalità delle cellule insulari. La disfunzione delle cellule β è inizialmente reversibile, una volta ridotte le
concentrazioni di glucosio con l'insulinoterapia, ma molti studi dimostrano che la tossicità da glucosio può
causare una perdita irreversibile di tali cellule. Sono necessarie 1-12 settimane perché le cellule β possano
riprendersi dall'intossicazione causata dal glucosio e perché la guarigione possa avvenire devono ridursile
concentrazioni del glucosio ematico e degli acidi grassi liberi. L'insulina è il più potente tra gli agenti capaci
di ridurre il glucosio, quindi occorre usarla quanto prima per aiutare la guarigione delle cellule β. Nel 20-
90% dei gatti con diagnosi recente, il diabete si risolve solitamente entro i primi 1-4 mesi di trattamento,
ma perché ciò possa avvenire, è necessario un controllo adeguato della glicemia affinchè le cellule β
possano riprendersi dall'intossicazione causata dal glucosio. I gatti guariti dal diabete possono presentare
ricadute settimane o anni più avanti, probabilmente a causa di condizioni concomitanti come perdita di
cellule β e insulinoresistenza.
Segnalamento: sono colpiti soprattutto animali di media età o anziani (maggiore prevalenza tra 7-10 anni),
la forma giovanile è molto rara e si sviluppa a meno di un anno di età. Mentre nel cane l'incidenza è due
volte maggiore nelle femmine rispetto ai maschi, nel gatto, invece, questi ultimi presentano una maggiore
predisposizione. Per quanto riguarda la razza, nel cane sembrano più predisposti Setter Irlandese, Barbone,
Yorkshire Terrier e Setter Inglese, nella specie felina il Burmese è la razza maggiormente segnalata.
Anamnesi: i segni che più frequentemente sono riportati dai proprietari sono poliuria e polidipsia, polifagia,
perdita di peso. Talvolta sono riportati anche infezioni ricorrenti, oppure segni clinici come anoressia,
vomito, diarrea, imputabili ad una concomitante pancreatite.
Visita clinica: lo stato di nutrizione è variabile. Nel gatto è segnalata debolezza/atassia sugli arti posteriori o
postura plantigrada (causata da neuropatia E' possibile rilevare un variabile grado di
disidratazione, pelo opaco e con forfora. Molto frequente nel cane è bilaterale. Nel gatto, alla
palpazione addominale si può rilevare un'epatomegalia dovuta alla lipidosi epatica.
Esame emocromocitometrico: di norma non evidenzia alterazioni. Se il soggetto è disidratato può essere
presente emoconcentrazione, mentre un aumento dei globuli bianchi può essere secondario ad un
processo infiammatorio in atto, soprattutto in caso
Esami biochimici: il reperto costante, è l'iperglicemia, con valori ematici di glucosio superiori a 200 mg/dl.
E' possibile inoltre riscontrare un aumento dei valori di ALT e fosfatasi alcalina (in genere <500 UI/l),
ipercolesterolemia, ipertrigliceridemia. Nei soggetti in condizioni gravi, che abbiano sviluppato
si evidenziano anchelettrolitici (acidosi metabolica).
Esame delle la glicosuria è l'alterazione più importante, essa indica che i livelli ematici di glucosio
sono superiori alla soglia di riassorbimento renale (180-200 mg/dl nel cane e i 200-300 mg/dl nel gatto). E'
possibile rilevare anche chetonuria,(conseguenza di un'infezione a carico delle vo di
un danno glomerulare secondario alla distruzione della membrana basale) e talvolta batteriuria associata o
meno a piuria o ematuria. Il peso specifico delle urine di norma è superiore a 1025 per la presenza di
glucosio.
Una volta formulata la diagnosi di diabete mellito, Naomi è stata subito sottoposta alla terapia insulinica
elemento cardine nella gestione di tale endocrinopatia. L'approccio terapeutico ha previsto l'utilizzo di
un'insulina suina lenta, somministrata due volte al giorno con un dosaggio iniziale di 0,25 UI/kg. E'
importante considerare che, la gestione terapeutica del diabete, prevede delle modifiche dei dosaggi in corso d'opera, di conseguenza aspetto basilare negli animali affetti da tale patologia, è il monitoraggio. Strumento indispensabile per il monitoraggio della terapia insulinica, è l'esecuzione di una curva glicemica, sebbene nel gatto, animale particolarmente suscettibile allo stress, la sua esecuzione può risultare difficoltosa, o comunque i valori ottenuti possono essere falsati dall'iperglicemia da stress. Una soluzione, possibile, è effettuare la curva glicemica a casa, per ridurre al minimo i fattori stressanti eventualmente con prelievo ematico dall'orecchio. Il monitoraggio, si deve inoltre avvalere dell'anamnesi, chiedendo al proprietario di misurare la quota di cibo e acqua assunti e se possibile monitorando l'emissione di urine. A due, tre settimane dall'inizio della terapia con l'insulina, è buona norma ripetere il dosaggio della fruttosamina sierica, che idealmente,in un soggetto in cui ci sia un buon controllo del diabete, dovrebbe rientrare in un range di normalità o essere poco al di sopra di esso. In base ai riscontri ottenuti con il monitoraggio, può rendersi evidente la necessità di modificare i dosaggi: andrebbero effettuate correzioni non superiori a 0,5 UI per dose ogni 7-10 giorni. Oltre alla somministrazione di insulina, la terapia di Naomi, ha previsto una dieta con prodotti specifici. Nel gatto diabetico, risultano ideali diete che abbiano un elevato tenore proteico e bassi livelli di carboidrati; poiché questo tipo di dieta può talvolta risultare poco appetibile, può essere utile scegliere un alimento umido al posto di quello secco. Poiché lo scopo principale della terapia dietetica, è quello di minimizzare l'effetto del pasto sulla concentrazione post-prandiale di glucosio, la razione quotidiana, andrebbe divisa in tale modo: metà delle calorie giornaliere dovrebbero essere fornite al momento dell'iniezione di insulina, mentre la quota rimanente dovrebbe essere distribuita in cibo sempre a disposizione dell'animale durante la giornata. Nel caso di Naomi, il monitoraggio effettuato a due settimane dall'inizio della terapia, ha evidenziato una leggera riduzione dei livelli ematici di glucosio, ma persistente glicosuria, e dall'anamnesi poliuria e polidipsia sono risultate persistenti. E' stato effettuato un incremento del dosaggio, e a un mese dall'inizio della terapia, curva glicemica, valori sierici di fruttosamina e analisi biochimiche, hanno evidenziato un notevole miglioramento delle condizioni del paziente. Naomi è tutt'ora in terapia, e monitorata a intervalli regolari, ma mostra un buon controllo del diabete mellito.
Diagnosi caso 10: E se l'anamnesi è muta….?
Il test IFAT ha messo in evidenza la presenta un titolo anticorpale pari a 1: 1280. La diagnosi formulata è stata quindi di Ehrlichiosi. L'Ehrlichiosi è una patologia causata da diverse specie di batteri Gram-negativi del genere Ehrlichia, a localizzazione intracellulare obbligata, ordine Rickettsiales, famiglia Anaplasmataceae, di cui fanno parte anche i generi Anaplasma, Neorickettsia e Aegyptiella. In particolare, il genere Erhlichia comprende le seguenti specie: E. canis, E. chaffeensis, E. ewingi, E. muris ed E. ruminantium, a loro volta raggruppate nel genogruppo E. canis. Tali batteri sono trasmessi dal morso di alcune zecche (Rhipicephalus sanguineus, Amblyomma americanum, Dermacentor variabilis) che hanno capacità infettanti nei confronti di diversi ospiti (cane, gatto, ruminanti, cavallo e uomo), all'interno dei quali infettano i globuli bianchi. L'ehrlichiosi monocitica canina (CME) è causata da E. canis ed è presente in tutte le aree temperate e tropicali del mondo (in Europa, in particolare, nell'area mediterranea), in relazione alla distribuzione geografica del suo vettore principale: Rhipicephalus sanguineus. I roditori selvatici e altri mammiferi non domestici rappresentano i principali réservoir per le zecche che infestano il cane e gli altri mammiferi ospiti; il cane, al contrario, non sembra costituire un serbatoio importante per il mantenimento dell'infezione in una determinata area. E. canis non è considerata patogena per l'uomo, poiché l'ehrlichiosi monocitica umana (HME) è sostenuta da E. chaffeensis. La trasmissione di E. canis
all'interno di Rhipicephalus sanguineus avviene per via trans-stadiale, mentre la trasmissione transovarica non è mai stata confermata. La zecca può infettarsi durante l'esecuzione di un pasto su un cane infetto indipendentemente dalla forma biologica assunta in quel momento (larva, ninfa, adulto), per cui Rhipicephalus sanguineus risulta infettante in qualunque stadio. La zecca assume il batterio dagli ospiti durante la fase acuta della malattia. Una volta infettata, può trasferire l'agente patogeno ad altri cani, durante i pasti successivi. Non è precisamente noto il tempo necessario affinché la zecca, durante il suo pasto, riesca a trasmettere il batterio all'ospite; i tempi medi riportati in letteratura variano da 4 a 48 ore. Altra possibile via di trasmissione può essere la trasfusione di sangue infetto, per cui i donatori dovrebbero essere sempre testati accuratamente per escludere la presenza del batterio nel sangue, con l'ausilio di tecniche biomolecolari (PCR). La trasmissione, in questo caso, avviene solo se il donatore è nella fase acuta (1-3 settimane) della malattia, quando cioè i batteri sono presenti nel sangue periferico all'interno dei globuli bianchi. Dopo la trasmissione all'ospite, E. canis si localizza all'interno dei monociti e dei linfociti, e più raramente nei granulociti neutrofili, attraverso un processo di fagocitosi. All'interno del sistema fago-lisosomiale i corpi elementari si replicano per scissione binaria fino alla formazione di aggregati batterici che assumono una forma definita "morula"; la conseguente morte della cellula ospite determina il rilascio dei corpi elementari, che possono infettare nuove cellule. Il principale meccanismo immunitario difensivo che si instaura nei confronti di Ehrlichia è una risposta di tipo T-helper 1 (Th1), caratterizzata dalla secrezione di interferone g (IFN-g), Tumor Necrosis factor a (TNF-a) e interleuchina 2 (IL-2), che induce l'attivazione di un'immunità cellulomediata. L'IFN-g rappresenta il modulatore chiave di tale meccanismo. L'attivazione della risposta immunomediata secondaria è cruciale nella patogenesi delle infezioni sostenute da Ehrlichia e nella comparsa di gravi squilibri immunitari indotti dall'agente patogeno e/o dal vettore. La maggior parte delle patologie sostenute da vettori è infatti caratterizzata da ipergammaglobulinemia, dalla produzione di immunocomplessi e autoanticorpi circolanti (per esempio, anticorpi antieritrociti, anticorpi antipiastrine, anticorpi antinucleo) che giocano un ruolo centrale nella patogenesi e nelle manifestazioni cliniche della patologia. In particolare, in corso di infezioni sostenute da E. canis è stata dimostrata la presenza di anticorpi antipiastrine, oltre alla presenza di anticorpi antieritrociti e antinucleo. I cani infetti, solitamente, non sviluppano un'immunità protettiva nei confronti di E. canis, per cui possono andare incontro a future reinfezioni; il trattamento terapeutico eseguito correttamente durante la fase acuta della malattia può contribuire, in alcuni casi, alla definitiva eliminazione del batterio dall'organismo. La CME è una patologia multisistemica clinicamente distinta in tre forme: acuta, subclinica e cronica. Può colpire cani di tutte le razze ed età, indipendentemente dal sesso. Può, però, manifestarsi in forme più gravi nel Pastore tedesco e nei soggetti di giovane età. La fase acuta ha un periodo di incubazione da 1 a 3 settimane ed è caratterizzata da febbre (anche superiore a 40 °C), anoressia, perdita di peso, letargia, congiuntivite, linfoadenomegalia, splenomegalia, trombocitopenia, leucopenia, lieve anemia e ipergammaglobulinemia. La tendenza al sanguinamento, raramente presente in questa fase, si manifesta con la formazione di petecchie, ecchimosi, epistassi o emorragie mucose e, generalmente, è causata dalla grave trombocitopenia e dai disturbi dell'aggregazione piastrinica (trombocitopatia). L'infiammazione e il sanguinamento delle meningi possono causare segni neurologici, quali iperestesia, deficit dei nervi craniali e spasmi muscolari. Come già accennato, durante questa fase l'agente patogeno si divide e si distribuisce nell'organismo ospite all'interno delle cellule mononucleate. La fase acuta può risolversi spontaneamente nell'arco di 1-2 settimane, anche senza un trattamento terapeutico specifico. Dopo circa 2-4 settimane si sviluppa la forma subclinica. La fase subclinica è caratterizzata dal fatto che il cane si presenta apparentemente sano, a volte può persistere solo una lieve trombocitopenia. Questa fase può persistere per mesi, fino a un periodo di 3 anni. Durante questo periodo alcuni soggetti immunocompetenti possono eliminare il parassita; altri, invece, passano alla fase cronica dell'infezione.
La forma cronica rappresenta la fase più grave della malattia ed è caratterizzata da letargia, anoressia, perdita di peso, linfoadenomegalia, gravi disturbi dell'emostasi, splenomegalia, uveite, artropatie, nefropatie, disturbi neurologici e febbre (questi ultimi due meno frequenti). Le alterazioni clinico patologiche questa fase sono: piastrinopenia, ipergammaglobulinemia, proteinuria, aumento di ALT, ALP, urea e creatinina. Nei casi più gravi si instaura una severa depressione midollare, per cui la piastrinopenia è accompagnata da leucopenia e anemia non rigenerativa. Gli esami di laboratorio di base per un primo sospetto della malattia sono l'esame emocromocitometrico, il profilo biochimico sierico, l'elettroforesi delle sieroproteine e l'esame delle urine. È importante ricordare che, oltre a definire la gravità del quadro clinico, le alterazioni clinico-patologiche monitorate attraverso tali esami spesso precedono l'insorgenza dei segni clinici e aiutano a identificare la fase clinica della malattia. Tra le alterazioni più frequenti della fase acuta vanno ricordati il rilievo di trombocitopenia, leucopenia, lieve anemia di tipo normocromico-normocitico e la modificazione del quadro proteico sierico, con ipergammaglobulinemia spesso accompagnata da aumento delle frazioni beta e dalla diminuzione delle albumine, con conseguente modificazione del loro rapporto. Un'attenta valutazione citologica dello striscio di sangue periferico è importante in questa fase, in quanto, anche se raramente (meno del 10% dei casi), può permettere il rinvenimento di morule all'interno dei monociti. La probabilità di visualizzare le morule può aumentare sensibilmente esaminando il buffy coat, dove si concentra un numero maggiore di monociti. Durante la fase subclinica non si apprezzano alterazioni di rilievo, fatta eccezione per una transitoria piastrinopenia alla quale è difficile attribuire un preciso significato clinico. La fase cronica è la più grave
clinico-patologiche:
ipergammaglobulinemia, proteinuria, aumento di ALT, ALP, urea e creatinina e, nei casi più gravi, pancitopenia. Da quanto detto e dalla valutazione del quadro clinico ed analitico, Mary è stata inquadrata in fase cronica di Ehrlichiosi, ed in particolare in fase cronica moderata in quanto ancora assenti segni clinici gravi quali severa depressione midollare ed emorragie. Il trattamento terapeutico di elezione nei confronti di E. canis include l'impiego di tetracicline, in particolare della doxiciclina. In letteratura sono riportati diversi protocolli terapeutici; il più impiegato prevede la somministrazione di doxiciclina o di tetraciclina cloridrato alla dose di 10 mg/kg una volta al giorno per os, per 28 giorni consecutivi. La terapia instaurata nei soggetti in fase acuta o affetti da una forma cronica ancora moderata è in grado, nell'arco di 24-48 ore, di determinare un veloce ed evidente miglioramento clinico, caratterizzato in particolare dalla scomparsa della febbre e dal progressivo aumento della conta piastrinica che, generalmente, si normalizza nell'arco di 2 settimane dall'inizio del trattamento. La terapia può fallire quando il cane è già in una grave fase cronica, soprattutto se si è instaurata una severa depressione midollare o sono presenti segni clinici quali emorragie, immunodepressione o coinfezioni (babesiosi, bartonellosi, leishmaniosi). In questi casi è necessario instaurare terapie di supporto quali fluidoterapia, trasfusioni di sangue, anabolizzanti, glicocorticoidi. Purtroppo, soggetti affetti da forme croniche gravi e complicate, spesso, nonostante la terapia, vanno incontro a decesso. Mary ha risposto positivamente al trattamento terapeutico a base di doxiciclina e ad oggi è in fase di monitoraggio. Il monitoraggio del cane malato di Ehrlichiosi si basa, oltre che sulla valutazione dei segni clinici, sull'andamento della trombocitopenia. La risoluzione della trombocitopenia è generalmente indicativa di una risposta efficace alla terapia; la conta piastrinica, infatti, tende a migliorare già dopo 24-48 ore dall'inizio del trattamento terapeutico e, nella maggior parte, dei casi si normalizza nell'arco di 14 giorni. Se la conta piastrinica non aumenta entro 7 giorni, deve essere considerato un altro meccanismo patogenetico (processi immunomediati, coinfezioni). La conta piastrinica va quindi ripetuta 4-8 settimane dopo il trattamento per confermare la guarigione clinica e il successo terapeutico. Dopo un trattamento terapeutico di successo, il titolo anticorpale tende a ridursi e negativizzarsi in circa 6-9 mesi. La permanenza di titoli anticorpali per tempi così lunghi dipende, probabilmente, dall'altezza del titolo all'inizio del trattamento; titoli molto alti tendono infatti a ridursi più
lentamente. Va sottolineato, però, che la positività sierologica può persistere anche dopo trattamento terapeutico o guarigione spontanea e non sembra direttamente correlata con la presenza di segni clinici, specialmente in aree endemiche. In questi soggetti, generalmente, il titolo anticorpale si riduce progressivamente nel tempo fino a scomparire nell'arco di alcuni mesi (6-9 mesi). Allo stesso tempo, però, l'infezione può persistere in soggetti trattati e clinicamente asintomatici nei quali la positività sierologica rimane stabilmente presente anche per anni. Un altro limite è rappresentato dalla possibile cross-reazione sierologica con altre specie di Ehrlichia. La messa in evidenza di titoli bassi è esclusivamente indicativa di un'esposizione al batterio e, nella quasi totalità dei casi, non ha alcun significato clinico. Per questo motivo, probabilmente, il titolo anticorpale non può essere considerato un indicatore della risposta alla terapia. La PCR, in questi casi, potrebbe aiutare a distinguere i soggetti con infezione persistente da quelli in cui rimane nel tempo solo un titolo anticorpale positivo. Secondo il gruppo di studio dell'American College of Veterinary Internal Medicine, infatti, la PCR andrebbe eseguita 2 settimane dopo l'interruzione della terapia. Se la PCR risulta positiva, andrebbe ripetuto un trattamento di 4 settimane. Se anche dopo questo trattamento la PCR dovesse essere positiva, si dovrebbe considerare l'impiego di un protocollo anti-E. canis alternativo. Se, invece, il risultato della PCR dovesse essere negativo, il test andrebbe ripetuto dopo 2 mesi; se ancora negativo, l'eliminazione terapeutica del batterio deve essere ritenuta molto probabile.
Source: http://www.formazioneveterinaria.it/soluzionicasi2014/Oliva.pdf
ASAMBLEA LEGISLATIVA - REPUBLICA DE EL SALVADOR DECRETO Nº 218.- LA ASAMBLEA LEGISLATIVA DE LA REPÚBLICA DE EL SALVADOR, en uso de sus facultades constitucionales, a iniciativa del Presidente de la República por medio del Ministro de Justicia y oída la opinión de la Honorable Corte Suprema de Justicia, DECRETA, la siguiente: LEY DE NOTARIADO
Analysis on the Use of Synonymous Adverbs: Maybe, Perhaps, Possibly, Probably, and Likely Analysis on the Use of Synonymous Adverbs: Maybe, Perhaps, Possibly, Probably, and Likely The main objective of the current paper is to provide fuller definitions of five synonymous adverbs that express uncertainty: Maybe, perhaps, possibly, probably, and likely. In order to achieve this goal, 178 examples are collected from both spoken and written corpora and closely examined from semantic, stylistic, pragmatic, and syntactic points of view. The major findings are as follows: Maybe is used frequently in a casual context; perhaps is salient in its pragmatic use, such as hedges, when used in speech; possibly conveys a less degree of likelihood due to its theoretical property; probably frequently occurs with non-human propositions; and likely often accompanies good evidence and is the highest in the likelihood hierarchy. Observations under different perspectives are amalgamated to provide a clearer grasp of each adverb.



